Koncentrace odměrného roztoku
Koncentrace odměrného roztoku se vyjadřuje výhradně pomocí látkové koncentrace (mol/l). Roztoky, které mají koncentraci vyjádřenou jiným způsobem (např. procentuálně), nikdy neslouží jako odměrné roztoky a používají se pouze jako pomocné roztoky.
V platném lékopisu je odměrný roztok označen zkratkou VS, roztok který není odměrný, je označen RS (resp. RS1, RS2, …).
Titr odměrného roztoku
Přesná koncentrace odměrného roztoku se nazývá titr odměrného roztoku. Udává se s přesností na čtyři desetinná místa. To znamená, že údaj c = 0,12 mol/l neodpovídá titru odměrného roztoku, ale jedná se jen o přibližnou koncentraci. Titr v tomto případě musí být vyjádřen c = 0,1200 mol/l.
V některých laboratořích se stále ještě využívá možnost vyjádření titru pomocí faktoru odměrného roztoku. Pak musí být na štítku vyznačena přibližná koncentrace roztoku i faktor (např. c = 0,1 mol/l, f = 1,0450).
Faktor odměrného roztoku udává, jakému objemu roztoku přibližné koncentrace odpovídá 1 ml roztoku přesné koncentrace. Je to číslo bezrozměrné, musí být udáno s přesností na čtyři desetinná místa a jeho hodnota musí být blízká číslu 1. Roztoky silnější než přesné mají f > 1, roztoky slabší než přesné mají f < 1, roztoky přesné mají f = 1,0000. Vynásobením přibližné koncentrace roztoku faktorem se získá titr odměrného roztoku.
Příklad: Vyjádřete pomocí faktoru koncentraci roztoku c = 0,2045 mol/l.
(řešení: c = 0,2 mol/l, f = 1,0225)
Příprava odměrného roztoku
Odměrný roztok se připravuje s použitím odměrných baněk. Vypočítané množství látky se odváží na vážence a převede se do roztoku, který se v odměrné baňce doplní destilovanou vodou na celkový objem k rysce odměrné baňky. Roztoky kapalných látek se připravují ředěním koncentrovanějších roztoků.
Pokud je k přípravě roztoku použita látka, která má vlastnosti látky základní, provádí se odvážení přesně na analytických vahách a převedení do roztoku musí být kvantitativní. Pokud je k dispozici látka nestandardní, navažuje se na předvážkách a titr roztoku se musí stanovit experimentálně.
Český lékopis používá pro označení odměrných roztoků zkratku VS (např. Dusičnan olovnatý 0,1 mol/l VS).
Normanaly
Normanaly se používají pro rychlou přípravu roztoků o přesné koncentraci i z nestandardních látek. Jsou to roztoky, nebo pevné látky, které jsou dodávány v zatavených skleněných ampulích. Každá ampule má dvě křehká místa (prohlubně), která se prorazí úderem skleněné tyčinky. Vzniklými otvory se obsah ampule kvantitativně převede do odměrné baňky a doplní se rozpouštědlem na požadovaný objem.
Každý normanal musí být opatřený štítkem, kde je uveden vzorec látky, která je v něm obsažena. Dále musí být uvedena koncentrace odměrného roztoku, který vznikne po doplnění obsahu ampule na 1 litr. Pokud se jedná o látku, která je citlivá na světlo, musí být použita ampule z hnědého skla.
Standardní látky
Standardní látky mohou být nazývané také jako primární standardy, analytické standardy nebo základní látky. Jsou to látky, které musí splňovat tyto základní požadavky:
- Chemická čistota látky (stupeň čistoty p. a., minimálně 99,99 % čistoty)
- Přesně definované chemické složení
- Stálost při skladování (neměly by přijímat vzdušnou vlhkost, neměly by reagovat se vzdušným CO2, …)
- Jednoznačný stechiometrický průběh reakce se stanovovanými látkami
- Vyšší molární hmotnost pro snazší navažování
Roztoky, které jsou připraveny ze standardních látek, mají přesný titr, pokud při přípravě roztoku bylo postupováno naprosto předpisově (navažování na analytických vahách, kvantitativní převedení do roztoku, použití čistého nádobí, přesné doplnění hladiny k rysce, …).
Titr roztoku připraveného ze základní látky se nemusí stanovovat experimentálně, ale vypočítá se z přesné navážky.
Příklad: Při přípravě 250 ml roztoku standardní látky H2C2O4.2H2O (dihydrát kyseliny šťavelové) bylo odváženo 0,6545 g kyseliny. Spočítejte, jaký titr měl připravený roztok?
Řešení: M(H2C2O4.2H2O ) = 126,06 g/mol 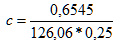
c = 0,0208 mol/l
Zdaleka ne u všech metod, které se v odměrné analýze používají, je možné pro přípravu odměrných roztoků použít standardní látku. Proto připravujeme odměrné roztoky (z nestandardních látek) rychlým, méně přesným postupem a titr takto připraveného odměrného roztoku stanovíme některým z dále uvedených postupů.
ČL používá pro označování standardních látek zkratku VR uvedenou za chemickým názvem.
Stanovení titru odměrného roztoku
Titr odměrného roztoku je možné stanovit některým z následujících postupů:
- Výpočtem z navážky
- S využitím standardní látky
- S využitím jiného odměrného roztoku se známým titrem
Stanovení titru výpočtem z navážky
Tuto metodu lze použít pouze u standardních látek a byla popsána v předchozí kapitole
Stanovení titru pomocí standardní látky
Pro tuto metodu je nutné mít k dispozici standardní látku, která kvantitativně reaguje s odměrným roztokem, jehož titr se stanovuje. Je možné titrovat buď navážku standardní látky (rozpuštěnou v malém množství vody), nebo ze standardní látky připravit roztok přesné koncentrace.
Odměrný roztok se připraví pouze v přibližné koncentraci, protože ani v případě sebepečlivější přípravy není možné docílit toho, aby roztok z nestandardní látky měl přesně požadovanou koncentraci.
Při všech výpočtech titrací je vždy naprosto nutné vycházet ze správně sestavené chemické rovnice, která popisuje děj probíhající při titraci. Obecně je možné zapsat rovnici takto:
aA + bB → cC + dD
(velká písmena označují reaktanty a produkty, malá písmena vyjadřují látková množství)
Ve výpočtu se používá faktor titrace Ft (pozor, neplést s faktorem odměrného roztoku), který se vypočítá jako podíl látkových množství obou reagujících látek. Z praktických důvodů se doporučuje do čitatele zapisovat látku, jejíž parametry jsou počítané, a do jmenovatele látku se známými parametry.
Na základě znalostí z předchozího studia je možné vyjádřit látkové množství dvěma způsoby:
Který ze vztahů se použije, závisí pouze na zadání konkrétního příkladu.
Titrací navážky standardní látky
Na základě chemické rovnice, která popisuje reakci odměrného činidla se standardní látkou, se vypočítá navážka standardní látky. Toto vypočítané množství standardní látky se odváží na analytických vahách. Skutečná navážka se smí od vypočítané navážky lišit o ±10 %, skutečná navážka se zaznamená.
Odvážená standardní látka se rozpustí v malém množství destilované vody a převede se kvantitativně do titrační baňky. K vzniklému roztoku se přidá vhodný indikátor a obsah titrační baňky se titruje připraveným odměrným roztokem do barevné změny indikátoru. Množství přidaného odměrného roztoku se zaznamená a použije se spolu s navážkou standardní látky k výpočtu titru.
Titrací roztoku standardní látky
Ze vhodné standardní látky se připraví roztok o přesné koncentraci. Podíl tohoto roztoku (obvykle 10-20 ml) se přesně odměří do titrační baňky, přidá se indikátor a titruje se odměrným roztokem do změny zbarvení indikátoru. Spotřeba odměrného roztoku se zaznamená a spolu s údaji o roztoku standardní látky se použije k výpočtu.
Pomocí jiného odměrného roztoku, jehož titr je známý
Využívá se v případě, že není k dispozici vhodná standardní látka, ale je k dispozici odměrný roztok s přesným titrem, jehož činidlo reaguje s činidlem odměrného roztoku nepřesné koncentrace. (Například pro stanovení titru roztoku HCl je možné použít odměrný roztok NaOH, jehož titr je již známý z předchozího stanovení.)
Postup a princip výpočtu je obdobný, jako v předcházející kapitole
Úprava titru
Z ryze praktických důvodů se skutečný titr nemá lišit od požadované hodnoty o více než ± 10 %. Větší odchylka by mohla způsobit neúměrně vysokou (nebo nízkou) spotřebu odměrného roztoku při titraci a tím by se pochopitelně snižovala přesnost stanovení. Takové roztoky je potřeba upravit.
Pokud je titr příliš vysoký, musí se roztok zředit, u roztoku s nízkým titrem se musí dodat činidlo.
Po úpravě roztoku je nutné titr znovu stanovit experimentálně některým u uvedených způsobů.